الف) مقدمه
کیت سنجش پروتئین برادفورد یک کیت رایج برای سنجش و تخمین پروتئین است که توسط برادفورد در سال 1976 ابداع شد. زمانی که معرف برادفورد با محلول پروتئینی مخلوط می شود معرف رنگ کوماسی اسیدی از قهوه ای به آبی تغییر رنگ پیدا می کند بطوری که شدت رنگ به مقدار پروتئین موجود در محلول وابسته است. تعیین پروتئین موجود در محلول با مقایسه رنگ حاصل از پروتئین با غلظت معلوم (استاندارد) که یک مجموعه ای از غلظت های مشخص و معلوم آلبومین سرم گاوی (BSA) است، صورت می پذیرد. به علاوه کیت حاضربا بسیاری از مواد شیمیایی احتمالیموجود در محلول پروتئین از جمله عوامل احیاکننده رنگ ها، شلاتورها، بافرها، حلال ها سازگار است. سنجش پروتئین می تواند در کووت یا میکروپلیت ها انجام شود.
ب) مزایای کیت سنجش پروتئین برادفورد
1- معرف برادفورد بسیار پایدار است و آماده استفاده است.
2- روش کالریمتری (Colorimetric) است و تنها نیاز به دستگاه اسپکتروفتومتر یا میکروپلیت ریدر استاندارد دارد.
3- روش انجام آن ساده طراحی شده است.
4- بسیار سریع است و رنگ بلافاصله بعد از مخلوط کردن معرف با محلول پروتئین ظاهر می شود.
5- محدوده وسیعی از غلظت پروتئین را از µg/ml 1500-1 می تواند اندازه گیری کند.
6- نیاز به کووت کوارتز ندارد و با کووت پلاستیکی یا شیشه ای قابل اندازه گیری است.
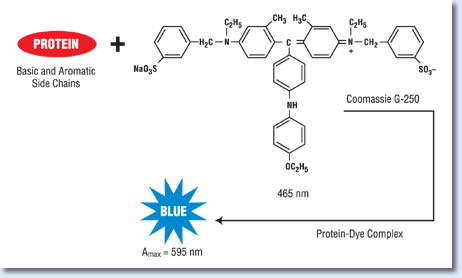
ج) اساس واکنش برادفورد
اتصال رنگ کوماسی بلو G-250 به پروتئین و تولید رنگ آبی که در طول موج 595 nm قابل کمیسازی است.تحت شرایط اسیدی کوماسی بلو G-250 به فرم کاتیونی است و رنگ آن قهوه ای می باشد در حالیکه در شرایط خنثی به رنگ سبز و فرم آنیونی آن به رنگ آبی می باشد. معرف برادفورد یک محلول اسیدی کوماسی بلو G-250 است و بنابراین به رنگ قهوه ای می باشد. زمانی که رنگ در مجاورت پروتئین قرار می گیرد، اولین الکترون خود را به گروه های باردار پروتئین می بخشد. بنابراین ساختار پروتئین تغییر یافته و بخش های هیدروفوب آن آشکار می شود. سپس رنگ از طریق گروه های سولفونیک اسید خود، شروع به اتصال به آمین های مثبت پروتئین میکند. مضاف بر آن، اتصالات از طریق نیروهای واندروالس نیز بین رنگ و پروتئین رخ می دهد. این اتصال های کوماسی بلو G-250 با پروتئین پایدار و آبی رنگ است.
تغییر رنگ کوماسی بلو G-250 از قهوه ای به آبی نسبت مستقیمی با غلظت پروتئین دارد و توسط اسپکتروفتومتر اندازه گیری می شود. معرف برادفورد در غیاب پروتئین دارای طول موج بیشینه 470 nm است. در حالیکه بعد از اتصال آن به پروتئین، همانند شکل زیر به 595 nm شیفت پیدا می کند. فرم سبز رنگ و خنثی کوماسی بلو G-250 که به پروتئین متصل نشده است، اما الکترون از دست داده است با سنجش برادفورد تداخل ایجاد نمیکند.زیرا جذب بیشینه آن 650 nm میباشد.
د) استانداردهای سنجش برادفورد
در روش برادفورد استانداردی برای کمّی سازی مقدار پروتئین در یک نمونه وجود دارد. استاندارد رایج برای روش برادفورد آلبومین سرم گاوی (BSA) و یا گاما گلوبولین گاوی (BGG) می باشد. بطور مطلوب و ایدهآل استاندارد میبایستی مقدار مشخصی از همان پروتئین که در محلول قرار است ارزیابی شود، باشد (استاندارد مطلق) اما برای بسیاری از نمونه ها امکان پذیر و عملی نیست به همین دلیل از BSA یا BGG استفاده می شود.
ه) محتویات کیت
و) نگهداری
معرف برادفورد و BSA را بعد از حل کردن در آب دوبار تقطیر میتوان به ترتیب در یخچال و 20- درجه به مدت یکسال نگهداری کرد.
ز) روش کار
بطور کلی می توان تعیین غلظت پروتئین به روش برادفورد را هم در لوله آزمایش و هم در میکروپلیت انجام داد. بر حسب شرایط، محقق یکی از روش های زیر را انتخاب کند.
1) پروتکل لوله آزمایش
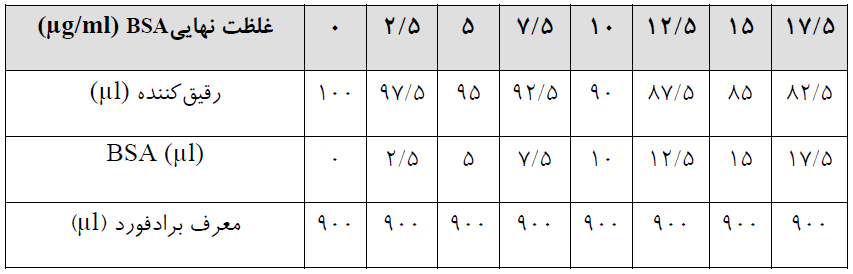
ابتدا غلظت mg/ml 1 محلول استاندارد BSA را تهیه کنید. بدین منظور کافی است مقدار کل mg5 از BSA که در کیت قرار داده شده است را در 5 میلی لیتر آب دوبار تقطیر حل کنید. سپس بر اساس جدول زیر در میکروتیوب یا لولهآزمایش شیشهای مقادیر زیر را تهیه کنید.
نکته:رقیق کننده میتواند آب مقطر باشد یا بافری که نمونه پروتئین در آن حل شده است.
پس از افزودن معرف برادفورد بعد از 5 الی 10 دقیقه میتوان جذب هر یک از آنها را در طول موج nm 595 خوانش کرد و نمودار آن را در نرم افزار Excel ترسیم کرد.
2) روش میکروپلیت
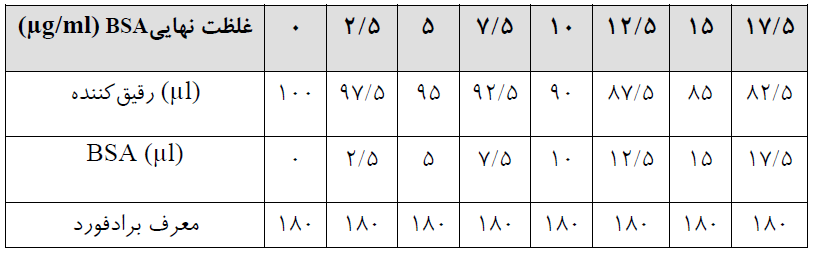
در این روش مقادیر مورد نیاز برای تهیه منحنی استاندارد به یک پنجم تقلیل مییابد. به علاوه بدلیل آنکه برداشتن حجم حاصل از کاهش BSAبا خطای احتمالی مواجه می شود،کافی است که غلظت BSA استاندارد، بجای mg/ml 1، mg/ml 2/0 تهیه شود. بدین منظور کافی است µl200 از BSA روش استاندارد با µl800 آب مقطر رقیق شود و سپس مقادیر زیر همانند جدول فوق تهیه و سپس در طول موج nm 595 خوانش شود.
نکته 1: حجم معرف برادفورد مورد استفاده در این روش 180 µl خواهد بود و رقیقکننده می تواند آب مقطر باشد یا بافری که نمونه پروتئین در آن حل شده است.
نکته 2: توصیه میشود برای هر یک از غلظتهای فوق حداقل دو تکرار انجام شود.
ح) محاسبه
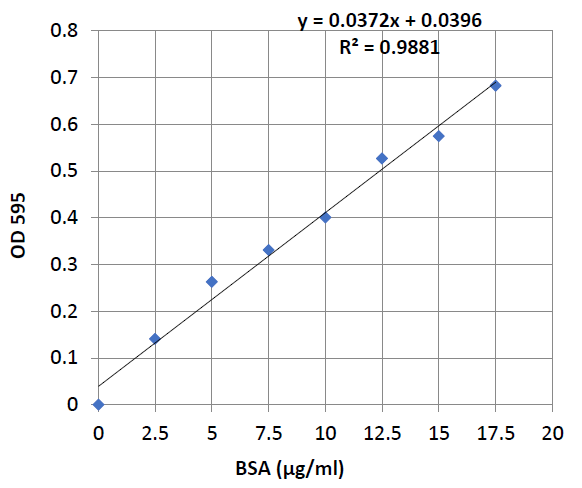
با ترسیم مقادیر استاندارد بر علیه عدد جذب آنها منحنی استانداردبه شکل زیر به دست میآید. بعد از ترسیم نمودار، برازش خطی (Trendline)، معادله خط و ضریب رگرسیون را نیز بر روی نمودار بهدست بیاورید.
ط) خوانش جذب نمونه یا نمونههای پروتئینی
برای تعیین غلظت نمونه(های) پروتئینی مقدار µl 10 از آن را با µl 90 آب مقطر یا بافر و µl 900 معرف برادفورد مخلوط کرده و بعد از 10 دقیقه جذب آن را در طول موج nm 595 قرائت و یادداشت کنید.
برای محاسبه غلظت محلول پروتئینی مجهول به کمک منحنی استاندارد کافی است عدد جذب نمونه پروتئینی را بجای y قرار دهید و مقدار x را پیدا کنید. سپس عدد حاصله را به عدد حجم پروتئین سنجیده شده ( در مثال فوق: 10) تقسیم و مقدار پروتئین بر حسب mg/ml یا µg/µl را بدست آورید. به طور مثال هرگاه مقدار جذب µl 10 از یک نمونه مجهول پروتئین 7/0 به دست آمد با استفاده از معادله بالا مقدار پروتئین بعد از محاسبه mg/ml 78/1 به دست میآید.
نکات:
1) توجه شود با هر دستگاهی که نمونه های منحنی استاندارد قرائت میشود با همان دستگاه جذب نمونه مجهول خوانده شود.
3) توجه شود که جذب نمونه های استاندارد بیشتر از عدد 8/. نباشد.
4) در صورتیکه مقدار جذب نمونه پروتئینی مجهول بیشتر از عدد 8/. باشد حجم پروتئین برای سنجش، کمتر انتخاب شود یا رقیق شود.
5) حجم پروتئین برای سنجش در روش لوله آزمایش تا µl 50 و در روش میکروپلیت تا µl 20 میتواند باشد. در صورتیکه با مقادیر فوق جذب بیشتر از 8/. شد، مقادیر کم شود.
ی) منابع