
الف) مقدمه
الکتروفورز یک روش آنالیزی در بیوشیمی و سایر علوم زیستی میباشد که برای جداسازی مولکولهای باردار در یک میدان الکتریکی به کار میرود. الکتروفورز ژل سدیم دودسیل سولفات پلیآکریلامید (Sodium Dodecyl Sulphate- Polyacrylamide Gel Electrophoresis) نوعی الکتروفورز است که در آن از سدیم دودسیل سولفات استفاده میشود تا تاثیر ساختار و بار مولکولهای پروتئین حذف گردیده و پروتئینها تنها بر اساس طول زنجیره یا وزن مولکولی تفکیک شوند. در این روش مولکولهای کوچک به دلیل مقاومت کمتر ماتریکس ژل سریعتر از مولکولهای بزرگتر حرکت میکنند و در نتیجه مسافت بیشتری را در ژل طی میکنند. SDS-PAGE یک سیستم الکتروفورزی ناپیوسته است که توسط لاملی ابداع شده است و توانایی تفکیک پروتئینها با وزن مولکولی حدود ۵ الی ۲۵۰ کیلودالتون را دارد. در سیستم ناپیوسته ژل دارای دو بخش ژل متراکم کننده (Stacking gel) با pH 6.8 و ژل جداکننده(Resolving gel) با pH 8.8 میباشد که در ژل متراکم کننده دارای منافذ بزرگتر، پروتئینهای بارگذاری شده تغلیظ و آماده تفکیک بر اساس وزن مولکولی در ژل جداکننده میشوند.
با وجود اینکه SDS-PAGE به دستگاه گران قیمت نیاز ندارد و روش انجام آن به نسبت آسان است، ولی، اهداف و کاربردهای آنالیزی گستردهای دارد. از جمله کاربردهای تحقیقاتی آن میتوان به تعیین درجه خلوص یک پروتئین، بررسی الگوی پروتئینی یک سلول، بررسی بیان یک پروتئین نوترکیب، تعیین وزن مولکولی نسبی یک پروتئین، اثبات حضور پیوندهای دی سولفیدی در پروتئینهای چند زیرواحدی، حتی تفکیک الیگونوکلئوتیدها و همچنین مرحله اول وسترن بلاتینگ اشاره کرد.
کیت حاضر شرکت آرسام فرا زیست برای الکتروفورز رایج پروتئین یعنی الکتروفورز در شرایط دناتوره احیایی تهیه شده است. محتوای کیت برای 25 و یا ۵۰ مینی ژل کافی است. صرفه جویی در زمان و هزینه های خرید مواد سازنده کیت، صرفه جویی در زمان تهیه و آماده سازی محلولهای سازنده، حذف هزینه آنالیز نمونه توسط شرکت های مربوطه و انجام الکتروفورز نمونه توسط خود محقق به خاطر روش کار ساده کیت از امتیازات ویژه کیت حاضر میباشد.
ب) محتوای کیت
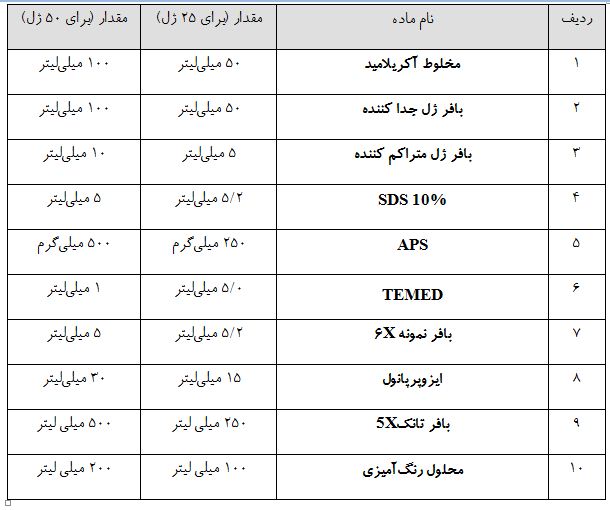
نگهداری کیت:
نکته:محلول 10% آمونیوم پرسولفات بهتر است به مقدارکم و تازه تهیه شود، به عنوان مثال میتوان mg ۵۰ ازآنرا در ml 5/0 آب دوبار تقطیر حل کرد.
موارد مورد نیاز که در داخل کیت موجود نیست:
- تانک الکتروفورز
- منبع تغذیه
- سرنگ همیلتون
- مارکر یا نردبان پروتئینی
- محلول رنگبری
ج) مراحل انجام آزمایش
۱) آمادهسازی ژل:
- ابتدا بر اساس مدل دستگاه الکتروفورز، شیشه ها و فاصله اندازهها را سرهم کرده و به نگهدارنده مخصوص متصل کنید. دقت شود که قبل از سرهم کردن شیشه ها آنها را کامل شسته و سپس با اتانول تمیز کنید. توجه شود که شیشه ها کاملاً روی هم قرار گرفته باشند.
- نکته: پس از سرهم کردن شیشهها، برای اطمینان از عدم نشتی میتوانید از آب مقطر استفاده نمایید. در صورت نیاز، برای درزگیری میتوان از آگار 1% استفاده کرد
- برای تهیه محلول ژل جداکننده ابتدا درصد ژل بر اساس جدول1 تعیین شده و سپس بر اساس جدول 2 مقادیر مشخص شده از هر محلول بجز TEMED را در یک ظرف تمیز ریخته و کاملاً هم زده شود. درست قبل از زمانی که میخواهید محلول ژل را به فضای بین شیشه ها منتقل کنید TEMED را افزوده، به هم زده و بلافاصله به فضای بین شیشه ها بریزید.
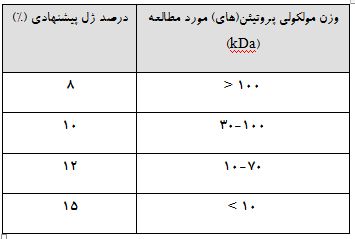
جدول 1: راهنمای انتخاب درصد ژل جداکننده بر اساس وزن مولکولی پروتئین های مورد مطالعه
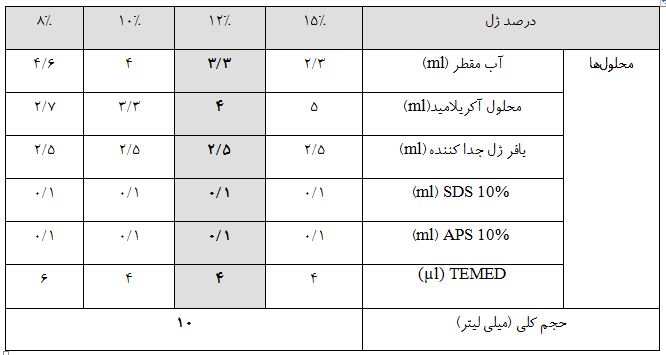
جدول 2: مقادیر مورد نیاز برای تهیه ژل جدا کننده با درصدهای متفاوت در حجم 10 میلی لیتر. در صورتیکه حجم ژل کمتری نیاز باشد میتوانید مقادیر آن را به یک نسبت کم کنید (ژل مورد استفاده در اغلب آزمایشگاه ها 12% میباشد).
- در حین انعقاد ژل جداکننده، مقادیر محلول ژل متراکم کننده به جز TEMED را مطابق جدول 3 درون یک بشر ریخته و کاملا هم زده شود. بعد از انعقاد کامل ژل جداکننده، سطح آن را با آب دوبار تقطیر شسته تا ایزوپروپانول آن حذف شود. پس از افزودن TEMEDطبق جدول 3 به محلول ژل متراکم کننده و مخلوط کردن آن، به آرامی محلول ژل را به فضای بین شیشه ها اضافه کرده و بلافاصله شانه تمیز را در داخل آن فرو کنید. بهتراست بعد از انعقاد ژل و قبل از در آوردن شانه، انتهای دندانه های آن را روی شیشه با ماژیک مشخص کنید تا نمونه گذاری و تشخیص چاهک ها راحت باشد.
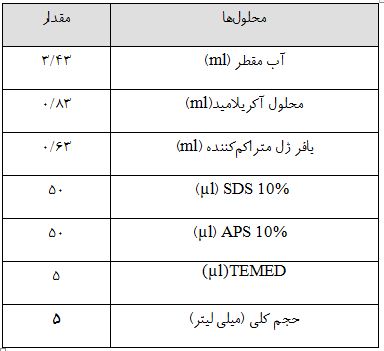
جدول 3: مقادیر مورد نیاز برای تهیه ژل متراکم کننده (۵ درصد)
۲) آماده سازی نمونههای پروتئینی
- نمونه های پروتئینی که میتوانند بر روی ژل بارگذاری شوند میتوانند مخلوط پروتئینی حاصل از لیزات سلولی، بافت یا پروتئین خالص از منابع گوناگون جانوری، گیاهی، قارچی، باکتریایی و ویروسی باشند. مقدار پروتئینی که میتوان بر روی ژل SDS-PAGE بارگذاری کرد مقدار 1 الی ۵ میکروگرم برای پروتئین خالص و 20 الی ۵۰ میکروگرم پروتئین ناخالص میباشد. برای تعیین غلظت آن می توانید از کیت سنجش پروتئین (روش برادفورد) شرکت ارسام زیست استفاده کنید.
- برای شروع کار بهتر است در یک میکروتیوب غلظت و حجم مشخصی از پروتئینهای خود را با بافر 6X مخلوط کرده (به عنوان مثال برای حجم ۲۵ میکرولیتر از نمونه ۵ میکرولیتر بافر نمونه 6X) و نمونهها را به مدت ۵-10 دقیقه در بن ماری با دمای ۱۰۰ درجه سانتیگراد قرار دهید. در این فاصله میتوانید ژل را به تانک متصل کرده و بافر الکترود تانک را تا پوشاندن سطح ژل و چاهکها به داخل تانک بالا و پایین بریزید. بعد از خنک شدن نمونه ها آنها را با سرنگ همیلتون و یا سمپلر در چاهک های ژل بارگذاری نمایید. از آنجایی که بافر نمونه دارای گلیسرول است نمونه در ته چاهک قرار میگیرند. توصیه میشود حجم یکسانی از تمامی نمونه ها در چاهکها بارگذاری شود. در صورت غلیظ بودن نمونهای آن را با آب مقطر رقیق کنید.
۳) انجام الکتروفورز
بعد از اتمام بارگذاری نمونه ها سیمهای رابط را به منبع تغذیه و تانک متصل کرده و الکتروفورز را در ولتاژ ثابت با شدت ۴۰-۳۰ ولت برای ژل متراکم کننده انجام داده و پس از رسیدن نمونهها به خط مرزی دو ژل، ولتاژ دستگاه را به 70-۵۰ ولت تغییر دهید. دقت شود که ولتاژ برای هر سانتیمتر طول ژل باید 10 الی ۱۵ ولت باشد که در این صورت برای مینیژلها حداکثر 100 و برای ژلهای متوسط و بزرگتر حداکثر 200 ولت خواهد بود.
۴) رنگ آمیزی و رنگبری
بعد از رسیدن رنگ آبی به انتهای ژل، الکتروفورز را متوقف کرده و با احتیاط ژل را از بین شیشه ها جدا کنید و بعد از شستشو با آب مقطر آن را در یک ظرف دربدار داخل محلول رنگ کوماسی بلو قرار داده و به مدت 30-۱۵ دقیقه رو شیکر قرار دهید. بعد از اینکه ژل کاملا رنگآمیزی شد محلول رنگ را خالی و برای رنگ آمیزیهای بعدی نگهداری کنید. ژل را با آب مقطر شستشو داده و سپس با اضافه کردن محلول رنگبر آن را به خوبی تکان دهید. باندهای پروتیئنی به تدریج به رنگ آبی ظاهر شده در حالیکه زمینه ژل بیرنگ خواهد شد. بعد از عکسبرداری و ثبت ژل میتوانید آن را در محلول %10 اسید استیک در یک ظرف درپوشدار برای مدت طولانی نگهداری کنید.
د) توصیهها
- در صورتی که دمای اتاق پایین است میتوان مقادیر TEMED و APS را تا دو برابر افزایش داد.
- حداقل 3 سانتیمتر از فضای بالای شیشه ها برای ژل متراکم کننده اختصاص داده شود.
- بلافاصله بعد از ریختن محلول ژل با یک سمپلر مقداری از محلول ایزوپروپانول به روی ژل اضافه کنید تا در موقع انعقاد ژل سطح آن صاف شود.
- از روی حجم کم باقیمانده محلول ژل در بشر میتوان به انعقاد ژل در فضای بین شیشه ها پی برد. متوسط زمان انعقاد ژل ۱۵ الی ۴۵ دقیقه خواهد بود.
- توصیه میشود که در مینیژلها ولتاژ نصف ولتاژهای گفته شده در بند 3 تنظیم شود تا بعد از رنگآمیزی باندهای شفافتری مشاهده شود.
۶) عیبیابی:
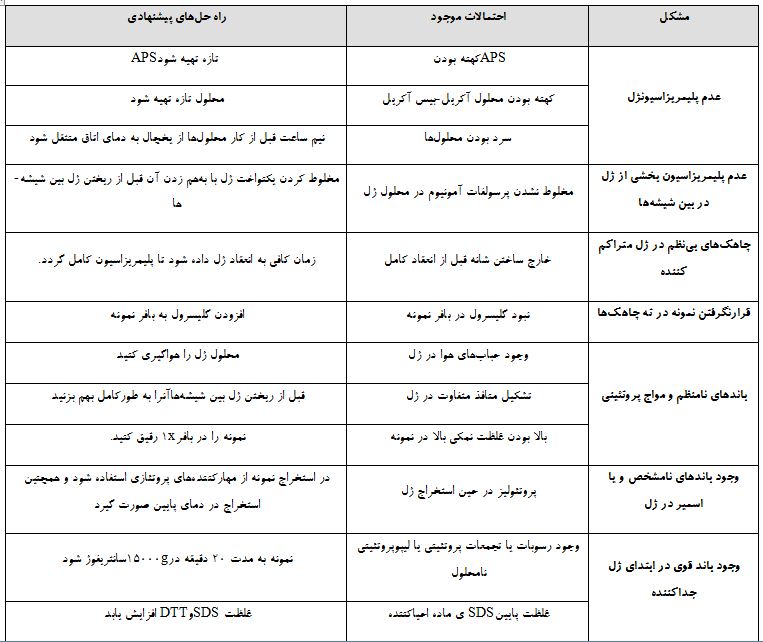
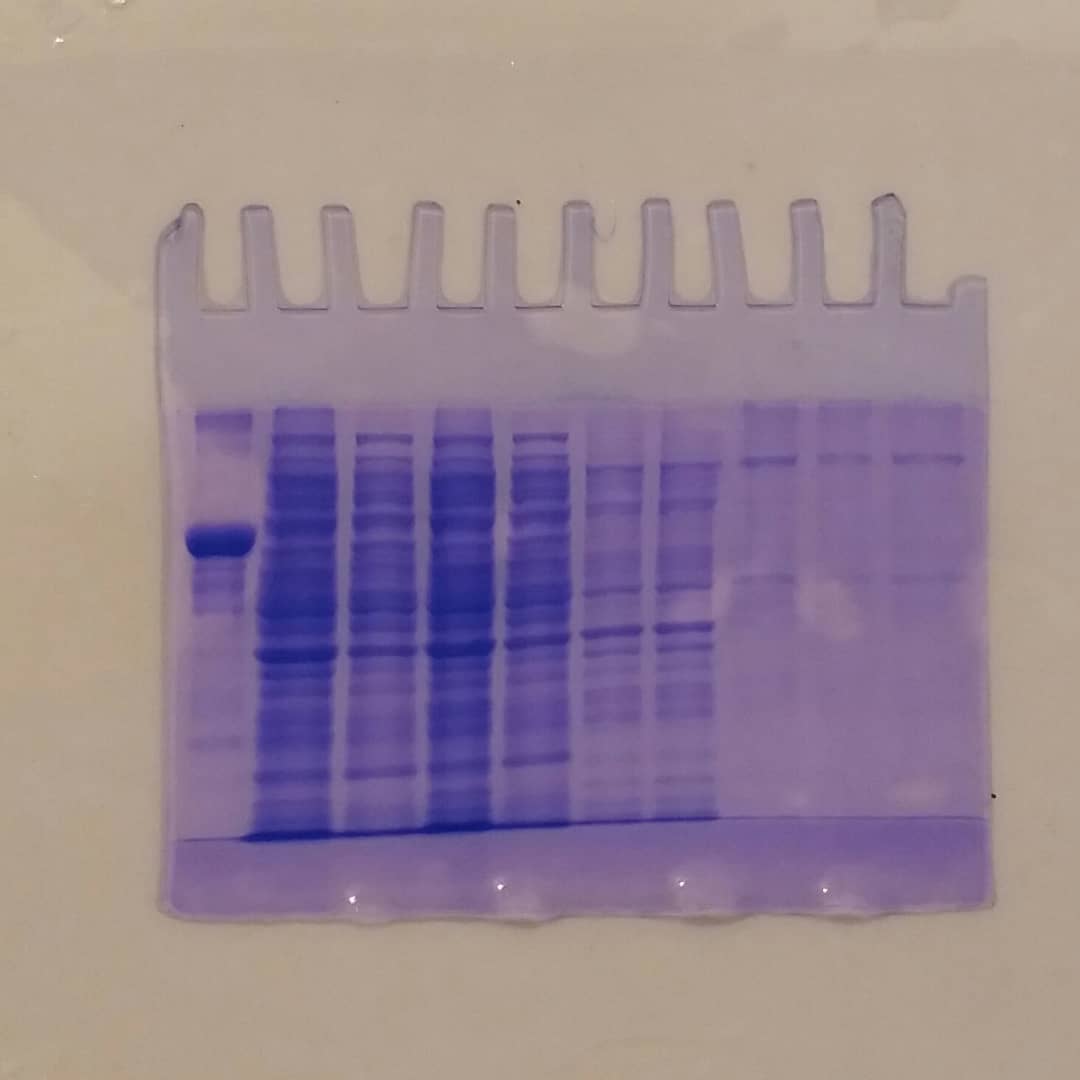

نمونه ای از ژل های حاصل از کیت SDS-PAGE شرکت آرسام فرا زیست


